Energia-sarja, osa 1: Mitä säteily on ja tarvitseeko sitä pelätä?
Modernissa yhteiskunnassa kuuluisi jo koululaitoksen tehtäväksi kertoa riittävät perusasiat siitä, mitä säteily on. Koska tuon tehtävän täyttäminen jää puolitiehen, moni ihminen kantaa aivan turhaan irrationaalisia pelkoja säteilystä ja ydinvoimasta. Toivottavasti tämä Päivän Byrokraatin uusi kirjoitussarja onnistuu hälventämään niitä edes vähän.
Kirjoituksemme säteilystä, samoin kuin energia-sarjan jäljemmätkin osat, on pyritty kirjoittamaan kansantajuisesti siten, että mitään keskeistä fysiikan termiä ei jätettäisi selittämättä. Jos selvisit koulumatematiikasta, selviät tästäkin. Tämä ensimmäinen kirjoitus ei kieltämättä ole kovin lennokas, mutta sen tarkoituksena on tarjota tarvittavia työvälineitä energia-sarjan tulevissa kirjoituksissa käsiteltävien ilmiöiden syvällisemmäksi ymmärtämiseksi.
Säteily liittyy ilmiönä siihen, että hieman yksinkertaistaen kaikki aine koostuu kahdenlaisista atomeista. On ensinnäkin sellaisia atomeja, joiden ytimessä on neutroneja saman verran tai korkeintaan hiukan enemmän kuin protoneja. Tällaiset atomit ovat sähköisesti tasapainossa ja ne ovat perusluonteeltaan stabiileja. Näitä atomeja kutsutaan myös pysyviksi tai tavallisiksi, koska ne eivät pyri hajoamaan, vaan pysyvät käytännössä ikuisesti muuttumattomina.
Sitten on atomeja, joiden ytimen neutronimäärä poikkeaa edellä kuvatusta. Puhutaan ns. stressatuista ytimistä. Tällaiset atomit ovat epästabiileja ja niiden ytimet voivat hajota itsestään eli spontaanisti. Tuon hajoamisen yhteydessä syntyviä tuotoksia kutsutaan säteilyksi, mutta malttakaa hetki – kerrotaan siitä kohta lisää. Tässä vaiheessa riittää, kun tietää, että jos aineen atomit ovat epästabiileja, ainetta kutsutaan sen hajoamistaipumuksen vuoksi radioaktiiviseksi.
Muutenkin, ennen kuin menemme asiassa eteenpäin, on hyvä tuntea sen verran fysiikan perusteita, että radioaktiiviset aineet eivät suinkaan ole pelkästään erilaisia eksoottisia ium-päätteisiä aineita, vaan radioaktiivisuus voi koskea alkuaineiden jaksollisen järjestelmän koko sfääriä.
Kun puhumme eri aineista, jaottelu tapahtuu sen perusteella, montako protonia kyseisen aineen atomiytimessä on. Esimerkiksi vedyllä on yksi protoni, heliumilla kaksi, litiumilla kolme, berylliumilla neljä, boorilla viisi, hiilellä kuusi protonia ja niin edelleen. Kysymys siitä, onko aine radioaktiivinen vai ei, ei ole pääteltävissä protonien lukumäärästä (eli siitä, mikä aine on kysymyksessä), vaan edellä jo mainituin tavoin aineen mahdollinen epästabiilius eli radioaktiivisuus on seurausta siitä, kuinka monta neutronia sen atomien ytimessä on.
Ja saman alkuaineen eri atomien ytimissä voi olla eri määrä neutroneja. Näitä saman alkuaineen erimassaisia atomeja kutsutaan toistensa isotoopeiksi.
Yksinkertaisimmalla alkuaineella, eli vedyllä on ytimessään aina yksi ainoa protoni, mutta siitä on neutronimäärän perusteella olemassa kolme eri isotooppia: ns. tavallinen eli kevyt vety, jonka ytimessä on vain yksi protoni eikä yhtään neutronia, raskas vety eli deuterium, jonka ytimessä on yksi protoni ja yksi neutroni sekä raskain vety tritium, jonka ytimessä on yksi protoni ja kaksi neutronia. Luonnon vetykaasussa nämä eri isotoopit esiintyvät hyvin eri suhteissa. Vetykaasu sisältää 99,99 % kevyttä vetyä, hieman vajaa 0,01 % deuteriumia ja 0,00000000000001 % tritiumia.
Hiilipohjaisina elämänmuotoina hiili on meille mahdollisesti keskeisin alkuaine. Myös sillä on useita isotooppeja.
Hiilellä on edellä todetulla tavallaan kuusi protonia ytimessään, mutta neutroneja hiiliatomeilla voi olla kuusi, seitsemän, kahdeksan tai jopa enemmän. Jos neutroneja on kuusi, tällaista hiiliatomia kutsutaan hiilen kemiallisen merkin C ja ytimessä olevien neutronien ja protonien yhteenlasketun määrän (6+6) perusteella isotoopiksi 12-C, ja jos neutroneja on seitsemän, isotoopiksi 13-C jne. Luonnossa esiintyy vain isotooppeja 12-C, 13-C ja 14-C, mutta myös suurempia isotooppeja saadaan aikaan keinotekoisesti.
Luonnossa esiintyvistä hiilen isotoopeista 14-C on radioaktiivinen, ja sitä on hengitysilman hiilidioksidin sisältämästä hiilestä 2,4 prosenttia. Ei mennä tähän aiheeseen tarkemmin, mutta tähän ilmiöön ja tunnettuihin puoliintumisaikoihin liittyy myös esimerkiksi fossiilien iän radiohiiliajoitus.
Erilaisia atomiytimiä tunnetaan yli 3100, ja näistä vain alle 300 on pysyviä eli stabiileja. Kaikki muut hajoavat ennemmin tai myöhemmin. Kun puhutaan puoliintumisajasta, tarkoitetaan aikaa, jonka kuluessa keskimäärin puolet tuon aineen atomeista on hajonnut spontaanisti. Mitä nurinkurisempi neutronimäärä on, sitä epästabiilimmaksi aine muuttuu, ja sitä nopeammin ydin tulee purkamaan ylimääräisen energiansa säteilypulssin muodossa.
Puoliintumisaika on luonteeltaan logaritmi, eli ko. ajan kuluttua radioaktiivisista ytimistä on jäljellä puolet, sitten puolesta puolet (1/4), sitten taas tästä puolet (1/8). Ajan funktiona radioaktiivisen aineen määrä lähestyy ikuisesti nollaa, mutta ei koskaan lakkaa kokonaan. Käytännön kannalta merkityksellisempi kysymys onkin, kuinka nopeasti aineen aktiivisuus alenee turvalliselle tasolle. Tuohon kysymykseen palataan, kun kirjoitussarjamme käsittelee ydinjätettä.
Eri alkuaineiden puoliintumisajat vaihtelevat paljon. Lyhyimmät puoliintumisajat ovat sekunnin osia ja pisimmät satoja miljoonia vuosia.
Esimerkiksi hiiliydin, jossa on vain 5 neutronia (11-C), sietää olotilaansa keskimäärin vain n. 20 minuuttia. 10-C pysyy koossa keskimäärin 19 sekuntia ja 9-C vain sekunnin kahdeksasosan. Yhtä ylimääräistä neutronia hiiliydin sietää helpommin. Esimerkiksi yllä mainitsemamme luonnossa esiintyvä radioaktiivinen isotooppi 14-C hajoaa kyllä, mutta suhteellisen hitaasti. Se säilyy muuttumattomana keskimäärin tuhansia vuosia. Kahta ylimääräistä neutronia hiiliydin kestää vain pari sekuntia ja kolmea alle sekunnin.
Vastaavalla tavalla kaikista muistakin aineista löytyvät sekä stabiilit että radioaktiiviset isotoopit.
Vertailun vuoksi, lääketieteessä käytetyn jodi-131:n puoliintumisaika on noin kahdeksan päivää, ja ydinvoimaloissa käytetyn uraani-235:n puoliintumisaika on noin 700 miljoonaa vuotta. Uraani itsessään ei siis ole erityisen voimakkaasti radioaktiivista, mutta sen hajoamistuotteet ovat.
Spontaanin hajoamisen lisäksi atomiydintä voidaan toki myös epävakauttaa tarkoituksella, absorboimalla ytimeen ylimääräinen neutroni tai protoni.
Kun atomiydin hajoaa, yhdestä raskaammasta atomiytimestä syntyy joukko uusia (kevyempiä) alkuaineisotooppeja ja säteilyä, joka tarkoittaa ytimestä poistuvia alfahiukkasia, beetahiukkasia tai gammasäteilyä. Tässä kohtaa on syytä vetää hetki henkeä ja todeta, että Albert Einsteinia edeltävän klassisen fysiikan soveltaminen ei tästä eteenpäin enää riitä, vaan lukijan on pakko hyväksyä se tosiasia, että materia ja energia ovat pohjimmiltaan yhtä, ja kerrottavissa ydinreaktioissa sillä on myös käytännön sovellus: osa materian massasta muuttuu reaktiossa energiaksi.
Emme mene vielä tässä kirjoituksessa kaikkein keveimpiin alkuaineisiin ja niiden fuusioon, jossa asiat tapahtuvat energian sitoutumisen ja vapautumisen kannalta juuri päinvastoin, mutta kun raskaampien alkuaineiden atomiydin hajoaa kahdeksi tai useammaksi pienemmäksi, syntyvät atomit painavat hieman vähemmän kuin se ydin, josta ne syntyivät. Määrä, jolla niiden massa on vähentynyt, on reaktiossa säteilynä vapautunutta sähkömagneettista säteilyä, eli energiaa.
Ja nyt aletaan vihdoin päästä asian (ja atomin) ytimeen. Pahoittelut pitkästä alustuksesta, mutta teksti menee täysin hukkaan, jollei lukijalla ole käytössään tarpeellisia pohjatietoja.
Kun yleiskielessä puhutaan säteilystä, puhutaan iloisesti sekaisin sekä hajoavan ytimen lähettämästä hiukkas- että energiasäteilystä. Suomesta ei esimerkiksi taida löytyä yhtään sanomalehtitoimittajaa, joka tuntisi asian niin hyvin, että pystyisi artikkeleissaan kirjoittamaan säteilystä ilman massiivisiakin asiavirheitä. Ja kun myöhemmissä artikkeleissamme puhumme esimerkiksi ydinonnettomuuksista ja ydinjätteestä, käsitteiden oikea tuntemus muuttuu hyvin merkitykselliseksi.
Osin huono tietämys johtuu tietysti fyysikkojen ja insinöörien mielellään käyttämästä monimutkaisesta terminologiasta ja siitä, että he tapaavat kuvata asioita hyvin eksaktisti – vaikka joskus olisi syytä hyväksyä vähäiset epätäsmällisyydet ja kansantajuistaa sanomaa pienillä yksinkertaistuksilla.
Esimerkiksi, kuten edellä totesimme, atomin hajoamisessa vapautuvaa hiukkassäteilyä tavataan kutsua alfahiukkasiksi ja beetahiukkasiksi (tai alfa- ja beetasäteilyksi) mutta asia olisi puettavissa paljon ymmärrettävämpäänkin muotoon. Alfahiukkaset ovat käytännössä heliumytimiä ja beetahiukkaset joko vapaita elektroneja tai positroneja. Positronit ovat elektronin antihiukkasia, eli mielenkiintoisella tavalla itse asiassa antimateriaa.
Koska alfa- ja beetasäteily ovat materiaa, niistä puhutaan hiukkassäteilynä. Niiden lisäksi hajoamisreaktiossa vapautuu myös energiaa, eli sähkömagneettista säteilyä. Sitä kutsutaan gammasäteilyksi.
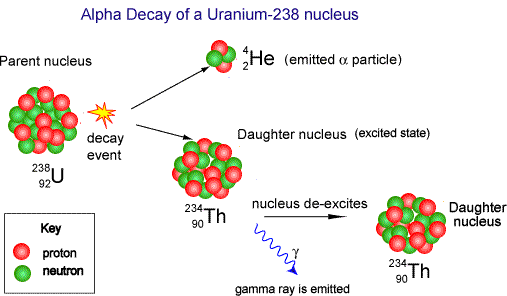
Kuvassa alfa-hajoaminen, jossa epästabiili uraani-238 -ydin hajoaa pienemmäksi thorium-ytimeksi ja helium-ytimeksi, eli alfa-hiukkaseksi. Samalla emittoituu gammasäteilypulssi.
Näiden lisäksi on kyllä olemassa vielä myös neutronisäteilyä, mutta koska sillä ei ole vielä tässä fysiologisessa aihepiirissä suurempaa merkitystä, hypätään nyt sen yli ja palataan asiaan, kun puhutaan siitä, miten ydinreaktio saadaan aikaiseksi.
Alfa-, beta- ja gammasäteilyä kutsutaan yleensä yhteiseltä nimittäjältään radioaktiiviseksi säteilyksi. Täsmällisemmältä luonteeltaan ne ovat niin sanottua ionisoivaa säteilyä. Tämä ionisointi on juuri se vaikutustapa, jolla säteily vaikuttaa meihin eläviin olentoihin. Ionisoinnilla tarkoitetaan sitä, että kun säteily kohtaa toisen atomin, ionisoiva säteily kykenee muuttamaan kohtaamansa atomin sähkövarausta, eli vaikuttamaan siihen, kuinka monta elektronia kyseisen atomin ydintä kiertää. Muutoksen eli ionisoitumisen seurauksena esimerkiksi kyseisestä atomista koostuva yhdiste voi hajota. Tällöin elävään soluun voi tulla vaurio tai mutaatio.
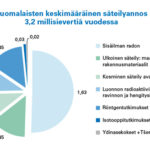
Koska juuri tässä kohtaa voi iskeä alitajuinen paniikki, lienee syytä panna rauhoittava käsi paniikkinappulan päälle. Suurin osa ionisoivasta säteilystä on joka tapauksessa luonnollista ja peräisin muualta kuin ihmisen toiminnan seurauksista. Kosminen säteily ja maaperän taustasäteily ovat suurimmat ionisoivan säteilyn lähteet. Säteilyn lääketieteellisen käytön (mm. röntgen) vaikutus on näiden jälkeen seuraavaksi suurin säteilyn lähde. Sen sijaan ydinvoiman ja ydinaseiden vaikutus on marginaalista pienempi, mutta näistä lisää seuraavassa artikkelissa.
Voidakseen vaikuttaa ihmiselimistöön, alfa- ja beetasäteilyn täytyy käytännössä päästä elimistön sisälle esimerkiksi hengitysilman tai ruoan mukana. Hiukkassäteilynä ne pysähtyvät muuten tehokkaasti pieniinkin esteisiin.
Esimerkiksi ihan tavallinen paperiarkki riittää pysäyttämään alfasäteilyn kokonaan. Alfasäteily ei pysty myöskään läpäisemään edes ihon ulointa, kuolleiden ihosolujen kerrosta ja pelkkä ilmakin pysäyttää sen niin tehokkaasti, että alfasäteily ei pysty etenemään ilmassa kuin muutaman senttimetrin.
Myös beetasäteily on helppo pysäyttää; siihen riittää alumiinifolio tai lasilevy. Suurin osa beetasäteilystä vaimenee jo ihan tavallisiin vaatteisiinkin, ja osuessaan paljaaseen ihoon, se kykenee tunkeutumaan enintään parin millin syvyyteen. Oikein suuri määrä beetasäteilyä voi aiheuttaa iholle päästessään palovamman – näin kävi muun muassa muutamalle kymmenelle palomiehelle, jotka osallistuivat Tshernobylin ydinvoimalan sammutustöihin reaktorirakennuksen alueella.
Miksi elimistön sisälle päästyään alfa- tai beetasäteily on sitten vaarallista? Siksi, että kehon sisällä ne pääsevät esteettä säteilyttämään hitaammin uusiutuvia kudoksia, joilla ei ole suojanaan kuollutta solukerrosta kuten esimerkiksi iholla. Tyyppiesimerkki on keuhkot, jonne pääsevä radioaktiivinen aines, kuten vaikkapa radon, luovuttaa energiansa läheisyydessään olevalle kudokselle ja voi aiheuttaa pitkän ajan kuluessa esimerkiksi syövän.
Jos olet miettinyt, miksi säteilyltä suojaudutaan valkoisilla haalareilla ja hengityssuojaimilla, ja ehkä myös ihmetellyt, että eikö säteily mene niistä helposti läpi, niin kyse on juuri suojautumisesta hiukkassäteilyä vastaan. Haalarin ja hengityssuojainten tarkoitus on estää nimenomaan ne tavat, joilla radioaktiiviset hiukkaset voisivat kulkeutua kehon sisään.
Energiasäteilynä gammasäteily taas toimii eri tavalla. Sähkömagneettisena säteilynä gammasäteily ei samalla lailla pysähdy kokonaan ainekerrokseen törmätessään, vaan se vaimenee ainekerroksen läpi edetessään vähitellen. Gammasäteilyn tapauksessa käytetään yleensä termiä puoliintumispaksuus, joka on säteilytehon puolittamisen riittävä ainemäärä, esimerkiksi betonin tapauksessa 6 senttimetriä. Lyijy on gammasäteilyn pysäyttämiseen vielä betoniakin tehokkaampaa; säteilytehon puolittamiseen riittää 1 cm lyijyä.
Mutta niinkin arkinen aine kuin tavallinen vesi käy hyvin eristeeksi. Kaikkein radioaktiivisimmankin, juuri reaktorista tulleen ydinjätteen gammasäteilyn turvalliseen eristämiseen riittää pari-kolme metriä vettä tai 35 senttimetriä terästä.
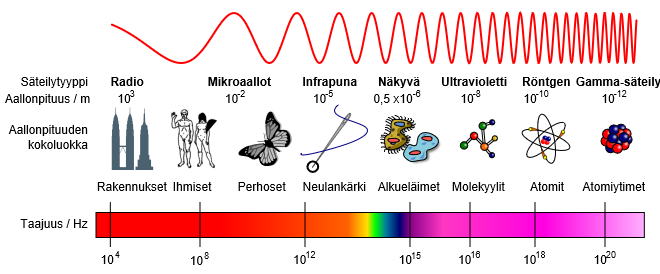
Valistunut lukija voi kysyä tässä vaiheessa, että hetkinen, eikös gammasäteily sähkömagneettisena säteilynä ole sitten käytännössä samaa asiaa kuin vaikkapa radioaallot? Kyllä. Ero syntyy vain tuon säteilyn sisältämästä energiamäärästä, joka radioaalloilla on vähäinen. Matalaenergiaisuutensa vuoksi radioaaltojen kyky läpäistä ainetta on korkeaenergistä gammasäteilyä parempi, ja siksi radioaallot etenevät jopa toiselle puolen maailmaa, ennen kuin ne vihdoin ovat absorboituneet ilmakehään. Mutta kyllä radioaalloillakin voi saada säteilyvammoja aikaiseksi. Jos kiipeät vaikkapa korkeaan tv-lähetystorniin sen ollessa käytössä, voit saada mastossa jopa tappavan annoksen säteilyä.
Toinen tapa kuvata hiukkassäteilyn ja energiasäteilyn eroa on se, että jälkimmäistä tavataan kansankielessä kutsua myös suorasäteilyksi. Jos olet säteilylähteen lähellä, saamasi gammasäteilyn määrä on suoraan laskettavissa etäisyydestä ja siitä, mitä ainetta sinun ja säteilylähteen välillä on. Ilmassa gammasäteily voi edetä enintään muutaman sata metriä. Läpitunkevalta gammasäteilyltä vaatetuksella ei luonnollisesti voi juuri suojautua.
Olet ehkä pannut merkille, että tässä kirjoituksessa ei ole yhtä poikkeusta lukuun ottamatta käytetty sanaparia ”radioaktiivinen säteily”. Se johtuu siitä, että radioaktiivista säteilyä ei varsinaisesti ole olemassakaan. On vain radioaktiivisia aineita, jotka hajotessaan lähettävät ionisoivaa säteilyä.













“…atomeja, joiden ytimessä on neutroneja saman verran tai korkeintaan hiukan enemmän kuin protoneja. Tällaiset atomit ovat sähköisesti tasapainossa ja ne ovat perusluonteeltaan stabiileja…”
Neutroni on varaukseton hiukkanen joka ei vaikuta atomiytimen sähköiseen “tasapainoon”. Ilmiön nimi on radioaktiivisuus jota kaiketi pyritään tekstissä tahallaan välttämään.
Toisekseen radioaktiivisessa aineessa voi olla myös liian vähän neutroneita.
“Valistunut lukija voi kysyä tässä vaihessa ……radioaallot? Ero syntyy vain tuon säteilyn sisältämästä energiamäärästä, joka radioaalloilla on vähäinen. Matalaenergiaisuutensa vuoksi radioaaltojen kyky läpäistä ainetta on korkeaenergistä gammasäteilyä parempi, ……” Tästä asiasta mentiin liian helpolla yli. Opettaja hyvä, voitteko ystävällisesti lisäselvittää vaikka Faradin häkin ?
Harri, artikkelin tiimoilta on N+200 asiaa, joista VOISI kirjoittaa yksityiskohtaisemmin. Silloin vaan artikkelista tulisi täysin lukukelvoton, eikä se enää lainkaan palvelisi päämääräänsä: luoda asiaa tuntemattomille hyvä yleiskuva ilmiöstä.